熟悉的一直是家中到學校的街景,這天,決定在市區亂亂『騎』~意外地在東興路上看到一間奇妙的建築物,『呀~玻璃屋,好像碳60球體!』

過幾天,在課堂上對學生提到起我的發現。『那間我去過,就在我家附近,』翔文說:『裡面賣衣服,還有一個大樓梯可以到二樓,它以前是賣咖啡的……』決定利用午休專程去拍照。原先還以為是預售屋,玻璃屋夾雜在一些建築物間,其實不算太顯眼,如果它的週遭是綠地或是白色建築,會更美~
走進門口看到鐵架,哦~原來是這樣搭建的。其實,它是由許多三角形玻璃窗所組合,,而且並非完全相同的等腰或正三角形;它的最頂端是由五片玻璃組成的五邊形,其他周圍則是六邊形,它,接近球體,但與碳60不同!

『妳看~』我手指著上方的幾何形狀:『有些是五邊形有些是六邊形,而且這些三角形並不規則。』
『原本沒注意這麼多,』她點點頭:『最近要加貼隔熱紙,請人來估價時,也注意到這點。』

經過銷售小姐請示經理許可,讓我在室內走動觀察拍照。這間採光很好,室內也佈置得很舒適,時值中午,幸好冷氣夠強,否則像溫室,鐵定會熱吧!『老師~下次再來,順便看一下我們的衣服!』ㄟ~這個嘛...再說啦~

國二上到有機單元,又在自然領域研習中看到碳60的模型,恰巧與我看到的玻璃屋,共同做個小文章整理一下。
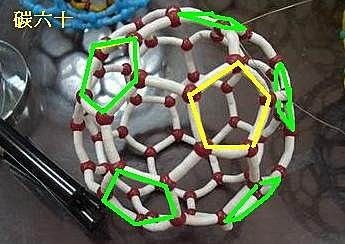
碳60、碳70其實是由五邊形與六邊形組合而成,結構要穩定,要有12個五個五邊形,上下六個(1個為頂~5個為輔)。以多面體結構來說,碳60為切角20面體,由60個碳原子組成,60個頂點,90個邊(60×3÷2=90,註)。共有32個面(12個五角形和20個六角形),我的算法:
(1)考慮共用點 60×3=180 (每個點被三個形狀共用)
(2)要組成一個封閉的球,上下要有12個五角形;12個五角形用去12×5=60個點
(3)180-60=120個頂點;120÷6=20 (20個六角形)
註:若用化學角度,計算鍵結形式,每一個碳原子,與相鄰的三個碳原子鍵結,90個邊,其中30個C=C雙鍵(由1個δ鍵及1個π鍵組成),60個C-C單鍵 (δ鍵)。每一個C以sp2混成軌域彼此鍵結形成單鍵,且均剩下一個pz電子,而每一個π鍵需2個pz電子,60個C有60個pz電子,故可形成30個π鍵。單鍵數目:90-30=60。
******
12個正五邊形,不僅能和20個六邊形構成C60,還可以和其他數目的六邊形組成蛋形的多面體,例如碳70。多年前曾在教甄中考過計算C60、C70的邊、面 (還包括五角形六角形數目)與鍵數,當時的我不會…現在這樣算,不知對不對?
我的參考計算:
碳70,70 個頂點,每個碳接3個,70×3÷2=105個邊,70pz÷2= 35個雙鍵,105-35=70個單鍵。
70個點 × 3=210;210-60=150 (12個五角形用去60個點);150÷6=25 (六邊形) ;共12個五邊形,25個六邊形。
如果想看切角20面體,碳60碳70與奈米碳管相關資料,最容易被搜尋到的資料便是國家高速網路與計算中心,張自恭博士 http://nano.nchc.org.tw/dictionary/c60.html
至於科博館大門的多面體,則是12個頂點,20 面體(均為三角形)。

原文發表於2008/04/21

